传统无机非金属材料有哪些(高中考点)
从化学角度看材料,材料分为金属材料、非金属材料、有机高分子材料、复合材料。
材料的分类
无机非金属材料主要用于传统工艺上面,比如水泥、陶瓷、玻璃以及耐火材料等,但它不断地焕发着新颜,对现代工艺发展,如建筑、国防、信息方面都具有重要的意义。
作为芯片材料的硅的设计和制造成为了我国重大发展的战略。无机非金属材料的主角——硅,同时也是高考化学中非金属元素的命题热点之一。
这部分教学安排比较孤立,是易被学生忽视和遗忘,本文通过梳理硅及其化合物的基础知识,供高中化学会考和高考的学生考前梳理加强记忆的准确性。

硅元素
硅元素在自然界的存在: 硅在地壳中的含量仅次于 氧 ,硅在自然界的存在形态: 只有化合态,没有游离态 (亲氧元素) 主要以 氧化物 和 硅酸盐 形式存在,是构成 岩石 和 矿物 的基本元素。

硅单质

硅晶体
单质硅也有 晶体 和 无定型 两种同素异形体,晶体硅的结构类似于 金刚石 ,它是带有金属光泽的 灰黑 色固体,熔点 高 ,硬度 大 ,有脆性,导电性介于 导体 和 半导体 之间,是良好的 半导体材料 用于做 计算机芯片 、光电池 。
在 常温 下化学性质 稳定 ,只能与 强碱 、氢氟酸 反应, 高温 下与 氧气 、 氯气 、 碳 等反应。
二氧化硅

石英晶体
(一)存在和用途:天然二氧化硅的存在形态有 晶体 和 无定型 两大类,统称 硅石 。石英晶体是 结晶 的二氧化硅,具有不同晶型和色彩,其中无色透明的晶体就是通常所说的 水晶 具有彩色环带状或层状的称为 玛瑙 。 沙子 中含有少量的石英晶体。

光纤光缆
SiO2是现代光学和 光导纤维 的基本原料。石英制作石英玻璃、石英电子表、石英钟等;水晶常用来制造电子工业的重要部件、光学仪器、工艺品等;石英砂常用作制玻璃和建筑材料。
(二)物理性质:二氧化硅熔点 高 ,硬度 大 ,这些性质是由 正四面体空间网状结构 决定的。
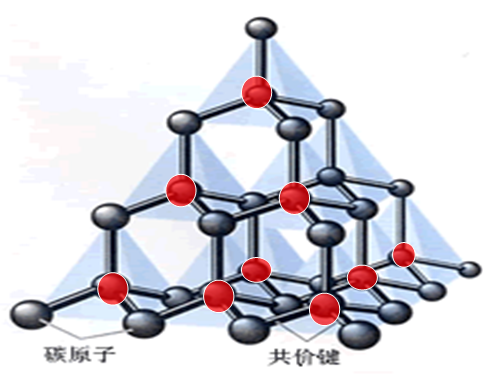
二氧化硅结构
(三)化学性质
(1)酸性氧化物通性:
SiO2与强碱反应,化学方程式为: SiO2+2NaOH==Na2SiO3+H2O ,离子方程式 SiO2+2OH—==SiO32—+H2O

实验室中盛放NaOH 溶液的试剂瓶用 橡胶 塞,而不用 玻璃塞 。
SiO2能与碱性氧化物反应: SiO2+CaO= 高温 ==CaSiO3
SiO2 不 溶于水, 不 与水反应
(2)SiO2的特性:
SiO2不与强酸反应,只能与 HF 反应,这是SiO2的特性。化学方程式为 SiO2+4HF==SiF4↑+2H2O 用于 刻蚀玻璃 。

(3)SiO2弱氧化性 SiO2+2C = 高温 =Si+2CO ↑ (二氧化硅制取单质硅的原理)

高纯硅的制法
注意:二氧化碳二氧化硅的异同
二氧化硅在 常温 只能与 强碱 、氢氟酸 反应, 高温 下与 碳 、 碱性氧化物 、碳酸盐 反应。
硅酸 (H2SiO3)
制备:硅酸是通过 可溶性硅酸盐 与 强酸 反应制得的
化学方程式: Na2SiO3+2HCl==2NaCl+H2SiO3(胶体) 、 Na2SiO3+CO2+H2O==H2SiO3(胶体)+Na2CO3

硅胶
硅酸的物理性质: 白色、胶状、难溶固体 硅胶的用途: 干燥剂、催化剂的载体 硅酸的化学性质:酸性: H2SiO3+NaOH = Na2SiO3 +H2O
不稳定性: H2SiO3 =加热= SiO2 +H2O
硅酸盐
硅酸盐是由 金属 、 硅 和 氧 组成的化合物的总称。硅酸盐大多 难 溶于水,化学性质 稳定 。 硅酸盐是构成 地壳岩石 的主要成分,种类多,结构复杂,常用氧化物的形式来表示组成。其表示方式: 活泼金属氧化物·较活泼金属氧化物·二氧化硅·水 。如:滑石Mg3(Si4O10)(OH)2可表示为3MgO·4SiO2·H2O
Na2SiO3 易 溶于水,其水溶液俗称为 水玻璃 ,可做 粘合剂 是 制备硅胶 和 耐火材料 的原料。

传统的硅酸盐制品有 陶瓷 、 玻璃 、 水泥 。
它们的原料分别为 黏土 、 纯碱、石灰石和石英 、 黏土和石灰石 。( 注意:只有陶瓷中没有石灰石原料 )
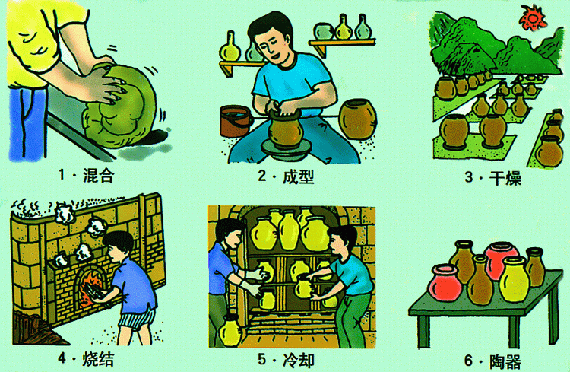
陶瓷烧制过程

水泥的制备

玻璃的制备
还有一些特殊功能的含硅物质有 碳化硅 (SiC,俗称金刚砂硬度大) 硅钢: (含4%硅),导磁性良好、 硅橡胶: 既耐高又耐磨。

硅单质及化合物之间的相到转化关系
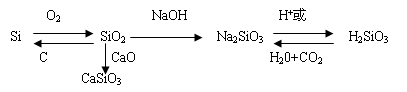
该类试题常以硅元素及其化合物知识为载体与化学基本概念,基本理论及化学实验密切结合,从高考命题的变化趋势看,常与前沿科技成果结合于一体,偏重于实际应用。
特别对硅和其化合物的用途要记忆准确,对硅和二氧化硅化学性质中高温的条件要明确,文中划线部分和红字部分务必关注。祝你考试顺利,金榜题名!

发表评论:
◎欢迎参与讨论,请在这里发表您的看法、交流您的观点。